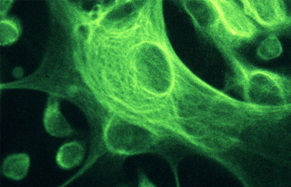
疾病中文名:vhl综合征
疾病英文名:Von Hippel-Lindau syndrome
别名:林岛综合征
患病率:1-9 / 100 000
遗传方式:常染色体显性遗传
ICD编码:Q85.8
VHL(Von Hippel-Lindau syndrome,VHL)综合征即小脑视网膜多发毛细血管瘤,是一种常染色体显性遗传的家族性肿瘤综合征,受累患者可在不同器官出现多种肿瘤,常见有脑血管母细胞瘤、视网膜血管母细胞瘤、胰腺囊肿、肾细胞癌(renal cell carcinoma,RCC)和(或)多发性肾囊肿以及肾上腺嗜铬细胞瘤等,其中中枢神经系统血管母细胞瘤和肾细胞癌危害最大。
概述1895年德国眼科医生Von Hippel发现视网膜血管母细胞瘤(Retina Hemangioblastoma,RHb)具有家族特性,1926年瑞典眼科医生Arvid Lindau也观察到视网膜和小脑的血管母细胞瘤是中枢神经系统(CNS)血管瘤病灶的一部分,并具有遗传性。到1964年,Melmon和Rosen总结了多篇临床报告,将CNS血管母细胞瘤合并肾脏或胰腺囊肿、嗜铬细胞瘤、肾癌以及外皮囊腺瘤等疾病正式命名为“Von Hippel-Lindau综合征”,简称VHL 综合征。
病因目前认为VHL综合征是由VHL基因的突变引起。VHL基因是一个抑癌基因,位于染色体3 P25区 ,编码含有214氨基酸,分子量为30 ku的细胞蛋白。VHL编码的蛋白参与构成一多蛋白复合体,可以负性调节低氧诱导的如血管内皮生长因子(VEGF) mRNA表达。VHL基因突变可造成该蛋白功能丧失,VEGF表达升高而发生富含血管的血管母细胞瘤。VHL基因突变在其它肿瘤发生中的机制尚未弄清。目前知道VHL基因不同位点的突变类型或称基因类型导致疾病的不同表现型,新生血管生成是肿瘤发生、发展的必要条件,散发肾细胞癌中也有70%发生VHL基因突变或高甲基化抑制。VHL基因突变的人群携带率估计为3/10万左右,外显率接近100%。其遗传特征为常染色体显性方式,子女有50%机率发病,故对其子女也应严密随访。
症状表现
VHL 综合征表现为一系列的病变,基本组成分为两部分:①视网膜、脑干、小脑或脊髓的血管母细胞瘤;②腹腔脏器病变(嗜铬细胞瘤、肾囊肿或肾细胞癌、胰腺囊肿等)。不同病变的组合其临床表现不相同。VHL综合征是根据视网膜和中枢神经系统两个以上不同部位的血管母细胞瘤或一个血管母细胞瘤伴有腹腔器官的病变而作出临床诊断。腹脏器官两个以上的病变或有家族史的患者有一个上述病变也要考虑该病的可能。诊断主要通过影像学检查和眼底检查。不同年龄段的患者上述病变发生率是不同的。如嗜铬细胞瘤常早发,而肾细胞癌很少在脑和眼底病变出现之前发生,但其后的发生率可高达70%。所以在临床工作中已诊断或有上述病变怀疑是VHL综合征的患者,应该定期随访,常规行B超或CT检查,以便早期发现病变。临床观察到VHL综合征的肾囊肿经过3~7年有恶变为肾癌的可能,所以肾囊肿应视为细胞癌的前体给予严密观察。
VHL综合征患者平均寿命不超过49岁。其主要死亡原因是中枢神经系统血管母细胞瘤破裂出血、肾细胞癌和嗜铬细胞引起的恶性高血压。中枢神经病变根据部位行手术或X刀、伽玛刀治疗。嗜铬细胞瘤应手术切除。肾细胞癌的治疗与散发性肾细胞癌有所不同,由于前者常为双侧多发,肿瘤生长较慢,转移较晚,故即使为单侧肾癌,也应尽量行保留肾单位的肿瘤切除手术,因为对侧也有在今后发生肾肿瘤的可能。多年临床观察发现,双侧全肾切除会诱发或加快其它部位的VHL肿瘤的生长,主要认为是由于移植术后的免疫抑制治疗和应用透析的结果。VHL综合征患者偶见有胰腺囊肿,遍布整个胰腺的小囊肿为其特征,如例2的表现。胰腺囊肿无恶变倾向,应不予处理。
诊断及分型:
VHL的诊断标准[23]:1、单发视网膜或中枢神经系统血管母细胞瘤伴有明确家族史,伴有嗜铬细胞瘤、肾脏、胰腺、附睾等部位的肿瘤 2、无明显家族史至少需两处视网膜或中枢神经系统血管母细胞瘤,或一处血管母细胞瘤伴内脏部位肿瘤。
分型:I型包括视网膜和中枢神经系统成血管母细胞瘤、肾囊肿、癌和胰腺囊肿,但没有嗜铬细胞瘤; II型包括视网膜和中枢神经系统成血管母细胞瘤,但另外存在嗜铬细胞瘤和胰腺的胰岛细胞瘤,既没有胰腺囊肿亦没有肾囊肿或癌;III型包括视网膜和中枢神经系统成血管母细胞瘤,嗜铬细胞瘤,胰腺和肾脏疾病。
治疗:
关于本病的治疗目前仍存在争论,Goldfarb[17]报道保留肾单位手术治疗VHL病肾癌,患者5年10年生存率分别为100%和81%,Roupret[18]报道56例行肾根治性切除或保留肾单位的手术,平均随访55.9月,其中17例复发,复发率为27.4%,复发病例中未见远处转移,5年生存率100%,10年生存率67%。也有行腹腔镜肾部分切除的报道,但术后18个月复发[19]。此种肾癌多为透明细胞癌,分级较低,恶性程度低,生长缓慢,几乎所有肾癌患者最终都将发展成双侧肾癌,该方法使患者在获得长无瘤生存的同时尽可能保留肾功能避免长期血透。术中疑为恶性囊肿者应切除,保留肾单位手术最大的问题是存在肿瘤残复发风险,对保留肾脏者,定期复查CT,如发现肿瘤局部复发,可再行保肾手术。VHL患者因其基因特点最终肾癌会复发,部分患者根治性双肾切除术以后可行肾移植术[20]或血透[21]。然而长期血液透析可引起较高的病死率,10年存活率仅为40%~67%,低于保留肾单位的手术。而且肾移植后长期服用免疫抑制剂,增加了肿瘤发生、复发、进展机会,肾移植需双肾切除后随诊2年以上,证实无肿瘤复发后方可进行。也有学者认为VHL病双侧肾癌的患者一侧行肾部分切除术,另一侧行根治性肾切除效果良好。如果肿瘤位于肾中央,则施行保留肾脏手术难度较大,应行根治性肾切除,保留肾单位的手术后应密切随访,每6~12个月行CT检查。
