
点击右上角![]() 微信好友
微信好友
 朋友圈
朋友圈

请使用浏览器分享功能进行分享

成纤维细胞生长因子(FGFs)及其受体(FGFRs)在人类胚胎发生、血管生成、细胞增殖和分化中起重要作用,随着FGFRs的异常活化,FGF/FGFRs信号通路几乎参与所有恶性肿瘤的发生和发展。FGF19与其受体FGFR4的过表达,通过激活无数下游信号通路,调控细胞的生存、增殖、侵袭和迁移等,诱发癌变。
在人类肝癌标本中,发现异常表达的FGF19和FGFR4与不良预后相关,过表达的FGF19参与肝癌的发展。在小鼠实验中,过表达的FGF19促进肝细胞增殖,导致肝细胞发育不良,诱发肝癌。使用FGFR4单克隆抗体,能抑制过表达FGF19小鼠中肝癌的形成和发展。近年来的研究中,通过阐述FGF19/FGFR4信号通路在肝癌中的关键作用,及其相关的分子靶向治疗,使得干扰FGF19/FGFR4信号通路成为一种治疗肝癌的新策略。
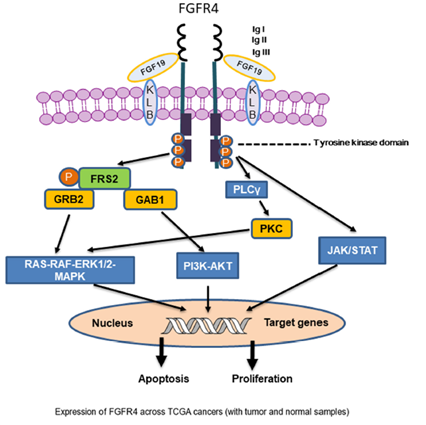
图片来源:Front.Cell Dev. Biol., 20 February 2020| https://doi.org/10.3389/fcell.2020.00095
实验证明,FGFR4多种疾病是有相关性的。FGFR4基因的表达抑制乳腺癌细胞克隆株的细胞凋亡,而阻断FGFR4基因的表达则出现相反的结果。Crose等的研究发现横纹肌肉瘤患者中有7%~8%的FGFR4激酶域活性在K535和E550两个位点有持续激活的突变,通过活化STAT3途径下游的信号通路,使其磷酸化AKT和EPK的能力下降,使肿瘤的侵袭性增加。Shimada等的研究发现,有三分之一的食管鳞状细胞癌患者有FGFR4的异常表达,而Zhou等的研究也显示80%以上的恶性外周神经鞘瘤患者中出现FGFR4的过表达,两者均提示患者的生存期缩短、预后不良。
FGFR4基因在胃癌、卵巢浆液性癌、结直肠腺癌中的过表达而呈现出较高侵袭性,抑制FGFR4基因的信号通路则可显著降低肿瘤的侵袭性,这提示FGFR4可作为肿瘤的潜在治疗靶标。Hagel等在对肝癌患者预后的研究中发现,大约30%的肝癌患者中有FGFR4基因异常高表达,且预后比较差。近年来的研究中,通过阐述FGFR4信号通路在肝癌中的关键作用及其相关的分子靶向治疗,使得干扰FGFR4信号通路成为一种治疗肝癌的新策略。小分子酪氨酸激酶抑制剂通过阻断胞内激酶与ATP结合的活性,阻断细胞增殖信号。FGFR4的小分子抑制剂可分为pan-FGFR抑制剂和FGFR4特异性小分子抑制剂。
从FGFR抑制剂毒副反应方面来看,由于缺乏选择性的pan-FGFR激酶抑制剂因脱靶而导致高磷酸盐血症、指甲脱离、脱发、黏膜炎、味觉障碍和黏膜干燥、结膜炎、角膜炎、眼睛干燥、无症状视网膜色素层剥离、骨关节疼痛、肌痛等不良反应,限制其临床应用。为了提高小分子抑制剂对FGFR4激酶域的选择性并减少不良反应,许多公司布局研发FGFR4选择性抑制剂。
SY-4798是首药控股自主研发的具有完全知识产权和全新化合物结构的新一代选择性FGFR4小分子抑制剂,综合临床前系统的药理学、药代动力学、毒理学研究结果,可以确认SY-4798是一个高活性的选择性FGFR4小分子抑制剂。肝癌在中国属于高发癌种,约占全球发病率的50%,且目前治疗方法不甚理想,存在严重临床未满足需求。目前,国内外尚无针对FGFR4靶点的药物上市。
目前,我院正在进行“一项评价FGFR4酪氨酸激酶选择性抑制剂SY-4798在晚期实体瘤受试者中安全性、耐受性、药代动力学、药效学和有效性的I期研究”,研究已获得国家药品监督管理局(NMPA)及本院伦理委员会的批准。研究分两个阶段,剂量递增阶段入组晚期实体瘤患者(优先入肝细胞癌(HCC)患者),剂量扩展阶段入组FGF19阳性的HCC及其他肿瘤。 (李进医生团队供稿,李进教授系同济大学附属东方医院肿瘤医学部主任、亚洲肿瘤联盟主席、中国临床肿瘤学会前理事长)
